DESCRIPCIÓN GENERAL: PARTE A
DESCRIPCIÓN GENERAL: PARTE B
El objetivo de la Parte B es examinar el tratamiento con el fármaco del estudio cada 4 semanas en las dosis seleccionadas en función de los datos de la Parte A. Hay dos cohortes en la Parte B: (1) participantes con tratamiento previo que recibieron previamente el tratamiento en investigación con SRP-5051 en la Parte A de este estudio o en el estudio 5051-102 y (2) participantes sin tratamiento previo recién inscritos en el estudio que no recibieron previamente el tratamiento en investigación con SRP-5051.
El estudio está cerrado a la inscripción.
Criterios de selección para los participantes sin tratamiento previo con SRP-5051
Es posible que su hijo sea elegible para participar en la Parte B del ensayo Momentum si cumple con los siguientes criterios de selección:
- Niños ambulatorios y no ambulatorios con distrofia muscular de Duchenne (DMD) de 7 a 21 años sin tratamiento previo.
- Tiene un diagnóstico genético de DMD y una mutación de deleción fuera del marco de lectura del gen DMD que es susceptible al tratamiento de omisión del exón 51. Hable con su médico si no está seguro.
- Ha recibido una dosis estable de corticosteroides durante al menos 12 semanas o no ha recibido corticosteroides durante al menos 12 semanas antes de recibir SRP-5051.
- Tiene una función pulmonar (respiratoria) y cardíaca estables.
- No han recibido tratamiento con ninguna terapia de omisión del exón 51 dentro de las 12 semanas previas a la selección, ni con ninguna terapia genética experimental para el tratamiento de la DMD en ningún momento.
- No tiene antecedentes de hipomagnesemia dentro de las 12 semanas previas a la selección.
Los requisitos adicionales para la participación se revisarán con los participantes y sus familias durante el proceso de selección.
Preguntas frecuentes
-
¿Qué es un estudio abierto?
Abierto significa que el médico del estudio, los enfermeros, los cuidadores, el patrocinador y usted sabrán que está recibiendo el fármaco del estudio y a qué dosis.
-
¿Qué significa dosis múltiples ascendentes?
Múltiples significa que todos los participantes recibirán dosis del fármaco del estudio una vez cada 4 semanas durante todo el estudio. Dosis ascendentes significa que hay diferentes niveles de dosis del fármaco del estudio en la Parte A que aumentan de un grupo de dosis a otro.
-
¿Qué significa expansión de la dosis?
En la parte B del estudio, los participantes serán asignados a 1 de 2 grupos de dosis y, posteriormente, recibirán dosis del fármaco del estudio en función de su peso corporal.
-
¿Cuántos niños se inscribirán en este estudio y dónde se llevará a cabo?
Se prevé inscribir a aproximadamente 60 participantes en este estudio (-30 participantes que recibieron tratamiento previo con SRP-5051 y -30 participantes que no recibieron tratamiento previo con el fármaco del estudio), con centros del ensayo clínico previstos en Estados Unidos, Canadá y Europa. Se puede encontrar información adicional sobre la ubicación de los centros del ensayo clínico en ClinicalTrials.gov.
-
¿Cuánto dura el estudio?
Se espera que la participación de los participantes que se inscriben en la Parte B del estudio dure aproximadamente 2 años.
-
¿Se me pagará por participar?
No se les pagará a los participantes por participar en este estudio. Sin embargo, Sarepta pagará por adelantado o reembolsará los costos de viaje razonables asociados con la participación en el estudio, de acuerdo con la política de viajes aprobada del estudio.
-
¿Cuáles son algunas de las actividades que se requerirán para participar en este estudio?
Los participantes inscritos visitarán los centros del estudio para recibir dosis mensuales y someterse a las evaluaciones funcionales, las pruebas médicas y las biopsias musculares en los puntos temporales correspondientes durante el transcurso del estudio. Algunas visitas requerirán pasar la noche en el centro del estudio. Los participantes se someterán a análisis de laboratorio de seguridad en cada visita.
-
¿Por qué debe realizarse biopsias?
Este estudio medirá el cambio en la cantidad de proteína distrofina en el tejido muscular esquelético después del tratamiento del estudio. Dado que estamos realizando pruebas para determinar si el SRP-5051 aumenta los niveles de distrofina en el tejido muscular esquelético mediante la omisión de exones, la única manera de mostrar que el SRP-5051 está funcionando como se pretende es analizar el tejido muscular esquelético directamente. Esto no puede estudiarse mediante un análisis de sangre u orina, por ejemplo. El centro del estudio proporcionará más información.
-
¿Qué riesgos están asociados con este estudio?
Al igual que con todos los estudios clínicos, puede haber riesgos asociados con los posibles efectos secundarios de tomar el fármaco del estudio y con las pruebas médicas estándar que se realizan como parte del estudio en cada visita. La información sobre los posibles efectos secundarios que pueden experimentarse en el estudio está disponible en el formulario de consentimiento y debe analizarla con su médico del estudio.
-
¿Cuáles son algunos de los beneficios de participar en este ensayo clínico?
Se desconocen los posibles beneficios de SRP-5051 en personas con DMD. Incluso si usted no se beneficia de participar en este estudio, podríamos aprender algo que podría hacer avanzar la investigación y ayudar a otras personas.
SareptAlly es un servicio de compatibilidad de participantes de ensayos clínicos para estudios patrocinados por Sarepta.
Un orientador de pacientes puede ayudarle a comprender sus opciones de ensayos clínicos.
Omisión de Exón para Duchenne
Acerca de la enfermedad de Duchenne
La enfermedad de Duchenne es un trastorno genético poco frecuente que acorta la vida de los niños y hace que sus músculos se deterioren y pierdan fuerza con el tiempo. La enfermedad de Duchenne es causada por errores específicos (mutaciones) en el gen que codifica la distrofina. La distrofina es una proteína que desempeña un papel clave en la función de las células musculares y las protege de los daños cuando los músculos se contraen y se relajan. Estas mutaciones en el gen de la distrofina provocan la falta de proteína distrofina en los músculos. Sin suficiente distrofina, los músculos se debilitan gradualmente hasta que no pueden moverse en absoluto y, finalmente, se pierde la función respiratoria y cardíaca.
Acerca del SRP-5051
SRP-5051 es un fármaco en investigación diseñado para tratar la enfermedad de Duchenne en pacientes que tienen una mutación confirmada en el gen de la distrofina que puede tratarse mediante la omisión del exón 51. Utiliza una tecnología denominada omisión de exón.
Acerca de la Omisión de Exón
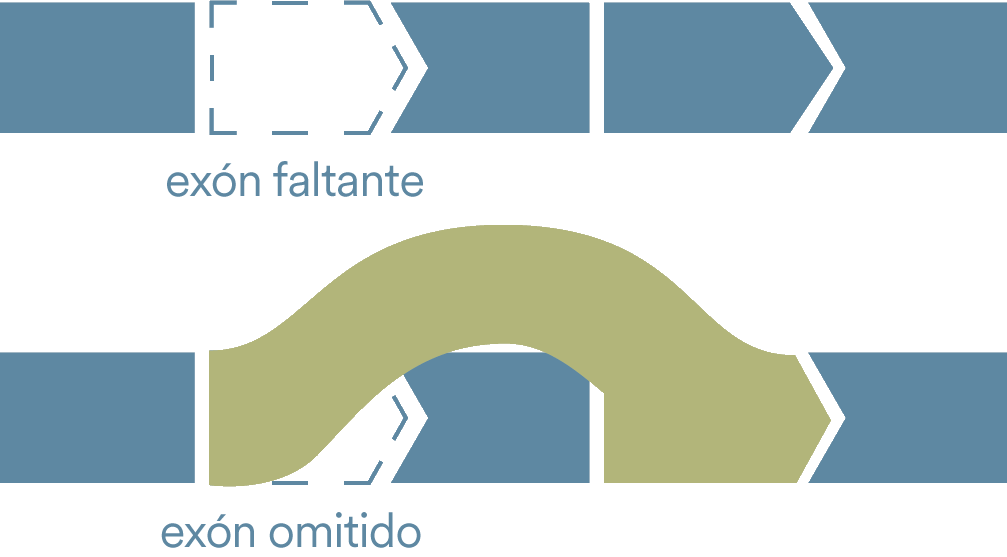 Las tecnologías de omisión de exón se esfuerzan por abordar el problema subyacente de la enfermedad de Duchenne: la falta de la proteína distrofina. Muchas personas con la enfermedad de Duchenne tienen una mutación genética en la que faltan uno o más exones en el gen de la distrofina. Esto provoca errores en las instrucciones para producir distrofina, dejando al cuerpo incapaz de producir la proteína.
Las tecnologías de omisión de exón se esfuerzan por abordar el problema subyacente de la enfermedad de Duchenne: la falta de la proteína distrofina. Muchas personas con la enfermedad de Duchenne tienen una mutación genética en la que faltan uno o más exones en el gen de la distrofina. Esto provoca errores en las instrucciones para producir distrofina, dejando al cuerpo incapaz de producir la proteína.
La omisión de exón le indica al cuerpo que oculte un exón junto a la pieza faltante para que se pueda omitir toda la sección y los exones restantes puedan encajar entre sí. El objetivo de la omisión del exón es permitir que el cuerpo produzca una forma más corta de la proteína distrofina.
Ubicaciones del ensayo
El estudio MOMENTUM prevé centros en Estados Unidos, Canadá, el Reino Unido y la UE. Para ver una lista actualizada de los centros del estudio globales participantes, visite clinicaltrials.gov

